Por que a Anvisa ainda não aprovou a CoronaVac?
Dois estudos já foram enviados, mas a Anvisa ainda aguardam um teceiro?
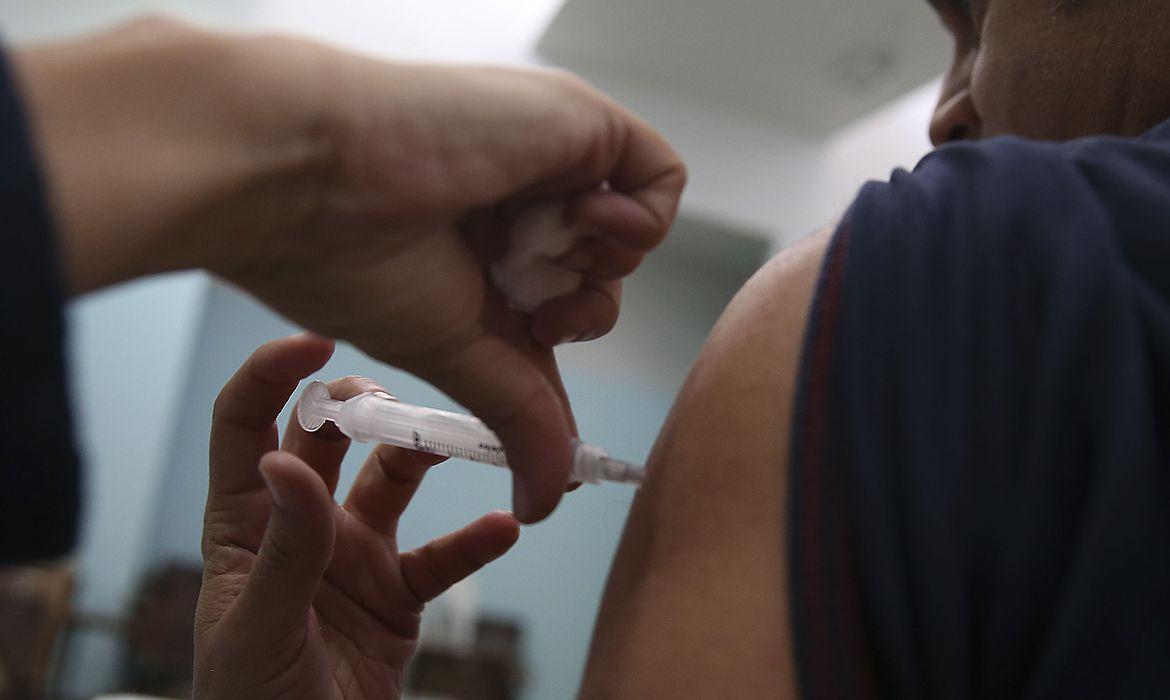 Anvisa: órgão alega que faltam algumas etapas para CoronaVac ser aprovada (Foto: Marcello Casal/Agência Brasil)
Anvisa: órgão alega que faltam algumas etapas para CoronaVac ser aprovada (Foto: Marcello Casal/Agência Brasil)
O que falta para a Anvisa aprovar a vacina?
- Estudos pré-clínicos: a primeira fase consiste em analisar de que forma o imunizante vai reagir no organismo do hospedeiro. Ela acontece antes mesmo do início dos testes em seres humanos;
- Autorização para estudos em humanos: para que os testes em humanos comecem a ser realizados, primeiro é necessário que a empresa ou o órgão que vai fabricar a vacina obtenha a aprovação dos Comitês de Ética em Pesquisa e/ou da Conep (Comissão Nacional de Ética em Pesquisa);
- Dossiê de Desenvolvimento Clínico de Medicamentos (DDCM): o DDCM consiste em um documento feito pela fabricante da vacina contendo informações detalhadas sobre ela e sobre seu estudo. Na Anvisa, o DDCM será analisado pelo Comitê de Avaliação de Estudos Clínicos, Registro e Pós-Registro de Medicamento, responsável por analisar o estudo pré-clínico e autorizar ou não o início da testagem em humanos;
- Estudos em humanos: o teste da vacina em humanos deve ser feito em três etapas (I II III) para verificar a eficácia da vacina. Cada uma delas cumpre objetivo diferente para o desenvolvimento da vacina;
- Pedido de registros de vacina: após passar por todo este processo, o fabricante deve solicitar o registro de vacina à Anvisa. Para isso, porém, terá que apresentar mais uma série de documentos, como o Certificação de Boas Práticas de Fabricação (CBPF), Autorização de Funcionamento (AFE), justificativa para o registro, plano de farmacovigilância e informações gerais sobre o produto e sobre sua matéria prima. Vacinas que estão na terceira fase de estudo em humanos já podem solicitar o registro, desde que seja comprovada uma alta eficácia do produto.
Atualmente, a CoronaVac está na terceira fase do estudo em humanos. Os documentos do primeiro teste realizado em voluntários foi enviado no dia 2 de outubro e a análise já foi concluída
Vacinação em SP deve começar dia 25 de janeiro de 2021
Veja o cronograma:
